来源:丁香园
这次“成功”,意义不只是验证一种药物的疗效和可行性。
原标题:重磅!新药有效延缓阿尔茨海默病进展,全球 III 期试验突破性结果发布
北京时间今天上午,针对早期阿尔茨海默病(Alzheimer’s Disease,AD)的 β 淀粉样蛋白(Aβ)抗体仑卡奈单抗(Lecanemab)大型全球验证性 III 期 Clarity AD 顶线(topline)结果,在美国旧金山举办的阿尔茨海默病临床研究大会(CTAD)上公开:
「试验药物 Lecanemab 在 1,795 名早期 AD 受试者中达到了主要终点和所有次要终点,且安全性表现符合预期。」

AD 高发、致死且无法逆转,首要治疗原则是早期干预
阿尔茨海默病,俗称「老年痴呆」,是 21 世纪以来最严峻的全球健康威胁之一。在中国,AD 死亡已上升至中国城乡居民总死亡原因中的第 5 位[1]。但目前临床上,尚无有效阻止 AD 发生或逆转其进展的治疗药物,AD 的治疗原则第一条就是「尽早诊断,及时治疗,终身管理」[2]。
轻度认知障碍(Mild cognitive impairment,MCI)阶段是 AD 早期检测、诊断和防治最为重要的窗口[3]。当前我国 60 岁以上老年人中约有 3,877 万 MCI 患者,其中 AD 源性 MCI 占 29.5%(约合 1,144 万患者)[3]。
对于 AD 源性 MCI 患者,目前一般推荐非药物干预。由于尚无用于 AD 源性 MCI 治疗的药物获批,临床也只能尝试应用现有的 AD 治疗药物来改善相关临床症状。以胆碱酯酶抑制剂多奈哌齐为例,临床上给 AD 源性 MCI 患者使用多奈哌齐以改善其步态并降低跌倒的发生率,但对于多数患者而言,目前批准用于 AD 症状治疗的药物在延缓 MCI 向 AD 进展以及综合获益方面的表现尚未明确[3]。

2022 年,AD 治疗药物研发历经低谷,终于看到希望
针对阻断或延缓 AD 病理进展的策略,可以被归纳为早期 AD 的疾病修饰疗法(Disease modified therapy,DMT)。
目前对 AD 的 DMT 药物的研发,主要基于对 AD 发病机制的两大假说——Aβ 假说(β 淀粉样蛋白过度生成并聚集成淀粉样斑块)和 Tau 蛋白假说(Tau 蛋白过度磷酸化后错误折叠形成神经纤维缠结),淀粉样斑块和神经纤维缠结相互协同导致脑细胞死亡引发 AD[4]。此外,对 AD 发病原因的推测还有如朊蛋白样传播假说、Aβ 和脑血管异常的相互作用、神经炎症假说等[3]。总的来说,目前学术界大多认为 Aβ 假说是 AD 病理生理的始动环节,而 AD 药物研发也常将 Aβ 清除作为主要的研发方向。
而 Aβ 在人类大脑中是以多种形式存在的,包括单体和不同大小的可溶性聚集体如寡聚体和原纤维,以及斑块中的不溶性 Aβ 纤维。一般认为可溶性 Aβ 聚集体具有较强神经毒性,例如 Lecanemab 靶向可溶性 Aβ 原纤维,多项研究表明 Aβ 原纤维具有神经毒性并促进疾病进展[5]。
距离 Aβ 假说提出至今已有 30 多年,但 AD 药物开发仍举步维艰。据统计,AD 药物研发失败率高达 99.6%,相比人类尚未攻克的另一难题——癌症,AD 的药物研发成功率仅是其 1/47[6]。
2022 年,AD 药物研发一再经历坎坷。自 2003 年以来全球只有两种 AD 新药获批上市,其中 2021 年刚在中国获得附条件批准用于改善轻中度 AD 临床症状的国产药物甘露特钠,于今年上半年宣布停止其国际 III 期临床研究[7];而 FDA 首个批准的 DMT 治疗药物 Aducanemab,也在今年宣布暂停欧洲上市申请[8]。
不久前,被寄予厚望的 Aβ 单抗 Gantenerumab 也宣布,两项针对早期 AD 的 III 期研究(GRADUATE I & II)未达到改善认知损伤的主要终点,其 Aβ 清除水平也低于预期[9]。
而在 2022 年结束前 1 个月,Lecanemab III 期 Clarity AD 临床研究积极结果的发布,让沉寂已久的 AD 药物研发领域终于迎来了一条振奋人心的好消息,也让 Aβ 假说终于「守得云开见月明」。
III 期 Clarity AD 研究:显著改善 AD 早期患者的认知下降,不良反应发生率符合预期
既往 Aβ 抗体药物研发有两大「拦路虎」——在大样本量患者群体中,Aβ 清除以及临床症状改善效果的验证,和不良事件的发生率控制在安全范围。而 Lecanemab 的 III 期临床试验达到了主要终点和所有次要终点,且淀粉样蛋白相关影像学异常(ARIA)总体发生率符合预期,提示其或许能安全有效延缓早期 AD 患者的疾病进展。

III 期 Clarity AD 研究结果显示,治疗 18 个月后,Lecanemab 治疗组与安慰剂组相比认知衰退幅度减缓 27%(差值 -0.45,95% 置信区间 [CI] -0.67 至 -0.23,P < 0.001),并达到了包括 PET 检测大脑中 Aβ 水平在内的所有关键次要终点;实际上,在治疗 6 个月时 Lecanemab 组就表现出与安慰剂组的显著差异,提示尽早接受治疗可以尽早获益[10]。
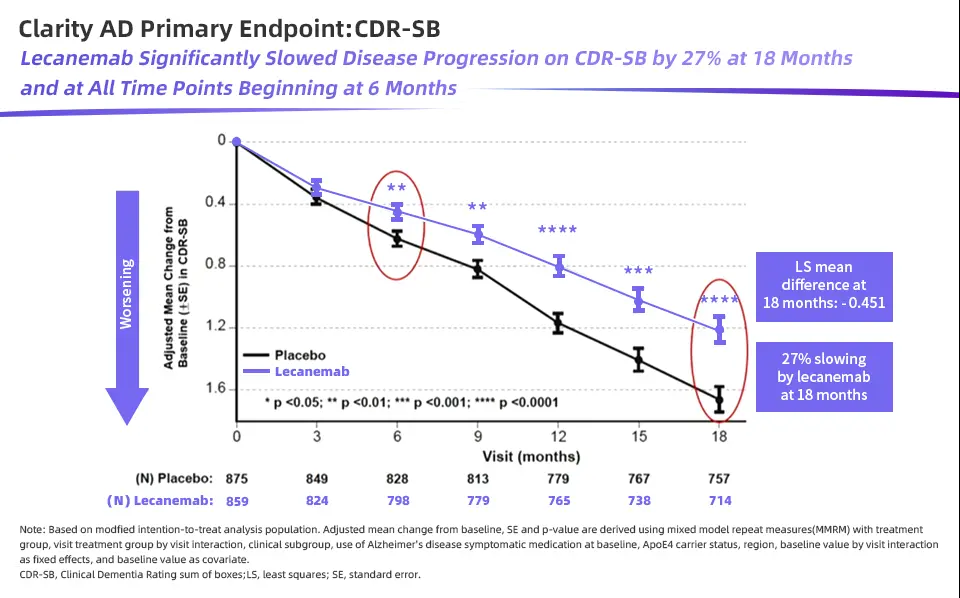
尤其是在清除 Aβ 水平方面,Lecanemab 治疗 3 个月时已出现显著差异,而在 18 个月后,与安慰剂相比 Lecanemab 可显著减轻脑内 Aβ 负荷(差值 -59.1 centiloids,95% 置信区间 [CI] -62.6 至 -55.6,P < 0.001),且 Aβ PET 平均值为 22.99 centiloids,低于 Aβ 阳性阈值(Aβ PET < 30 centiloids)[10]。

安全性方面,Lecanemab 组淀粉样蛋白相关影像学水肿(ARIA-E)发生率 12.5%(安慰剂组为 1.7%),淀粉样蛋白相关影像学出血(ARIA-H)发生率 17.0%(安慰剂组为 9.0%),Lecanemab 的 ARIA 总体发生率符合预期。III 期 Clarity AD 研究中,Lecanemab 治疗中最常见的不良事件是输液反应(Lecanemab 组 26.4% vs 安慰剂组 7.4%),而通过在输注 Lecanemab 前使用抗组胺药、皮质类固醇或抗炎药进行预防性治疗,63% 患者不再发生其他不良反应[10]。
CTAD 大会上研究人员 Takeshi lwatsubo 教授表示,「相关数据今日已发表于 New England Journal of Medicine(NEJM),目前美国 FDA 已接受了该药物生物制品许可申请(BLA)并授予优先审评资格,预计在 2023 年 1 月 6 日前做出决定」。

AD 疾病负担日益加剧,而积极预防、早期识别和干预,可以更好延缓疾病的进展
AD 是疾病负担最高的疾病之一。一项全国性研究显示,2015 年我国 AD 患者的年治疗费用为 1,677.4 亿美元,合约人民币 11,975.6 亿,预计到 2050 年将高达 18,871.8 亿美元,合约人民币 134,733.3 亿(按照 2022 年 11 月 30 日美元/人民币实时汇率计算)[1]。
除了治疗负担,AD 患者家属的照护压力也很大。《中国阿尔茨海默病患者诊疗现状调研报告》显示,区别于国外常见的机构养老,中国人群中六成以上为居家照护形式[11]。而 AD 患者晚期丧失独立生活能力,又难以沟通,照料起来甚至比照顾一个幼儿还要难。
随着人口老龄化问题日益加剧,临床、生活中 MCI 患者越来越常见,而这些患者数年后有一半可能会进展为 AD[3]。针对这一情况,积极采取一级预防措施,合理饮食、规律进行体力和脑力锻炼、良好睡眠、控制血压、防治如糖尿病、脑血管疾病、心房颤动等基础疾病等对 AD 源性 MCI 的预防有一定的帮助[3]。
而对于处于临床前期的 AD 患者(脑内 Aβ 沉积而暂无临床症状),目前尚无有效的药物治疗方案,以延缓 AD 典型临床症状的出现。而此次宣布 III 期临床「成功」的 Lecanemab 或许有希望改变这一局面,让更多 AD 源性 MCI 患者、临床前期 AD 患者延缓疾病进展,有机会享受更高质量的晚年生活。

致谢:
感谢北海道大学神经科学硕士、盛诺一家高级医学顾问 庄时利和 对本文做出的贡献。本文经由天津大学泰达医院神经内科主任医师 赵伟,江西省人民医院神经内科副主任医师 王明月 专业审核。
内容策划:王茉
项目审核:梁思
图表设计:孙兴兴
题图来源:图虫创意
参考文献:
[1]. Ren R, Qi J, Lin S, et al. The China Alzheimer Report 2022. Gen Psychiatr. 2022;35(1):e100751.
[2]. 国家卫生健康委办公厅. 阿尔茨海默病的诊疗规范(2020年版).
[3]. 中华医学会神经病学分会痴呆与认知障碍学组. 阿尔茨海默病源性轻度认知障碍诊疗中国专家共识2021[J]. 中华神经科杂志, 2022, 55(5):20.
[4]. Busche, M. A., & Hyman, B. T. (2020). Synergy between amyloid-β and tau in Alzheimer’s disease. Nature neuroscience, 23(10), 1183-1193.
[5]. Söderberg L, Johannesson M, Nygren P, et al. Lecanemab, Aducanumab, and Gantenerumab – Binding Profiles to Different Forms of Amyloid-Beta Might Explain Efficacy and Side Effects in Clinical Trials for Alzheimer’s Disease [published online ahead of print, 2022 Oct 17]. Neurotherapeutics. 2022;10.1007/s13311-022-01308-6.
[6]. Daunert S, Sittampalam GS, Goldschmidt-Clermont PJ. Twenty-First Century Diseases: Commonly Rare and Rarely Common?. Antioxid Redox Signal. 2017;27(9):511-516.
[7. 关于提前终止甘露特钠胶囊(GV-971)国际多中心3期临床研究的公告. https://mp.weixin.qq.com/s/GDlW4BR53GNVFPRZPOE2og ,核准时间 2022 年 11 月 24 日.
[8]. 渤健撤回阿尔茨海默病新药Aduhelm在欧洲的上市申请 https://mp.weixin.qq.com/s/zW8622sIYfszrD66t67nww ,核准时间 2022 年 11 月 24 日.
[9]. 罗氏皮下注射Aβ单抗治疗早期阿尔兹海默症两项III期研究未达到主要终点. https://mp.weixin.qq.com/s/tBD-e7pORQGxlJqMFVVsjA ,核准时间 2022 年 11 月 24 日.
[10]. Christopher H. van Dyck, M.D., Chad J. Swanson, Ph.D., , et al.Lecanemab in Early Alzheimer’s Disease. New England Journal of Medicine. DOI: 10.1056/NEJMoa2212948
[11]. 中国老年保健协会阿尔茨海默病分会. 中国阿尔茨海默病患者诊疗现状调研报告. 2021 年 4 月.
